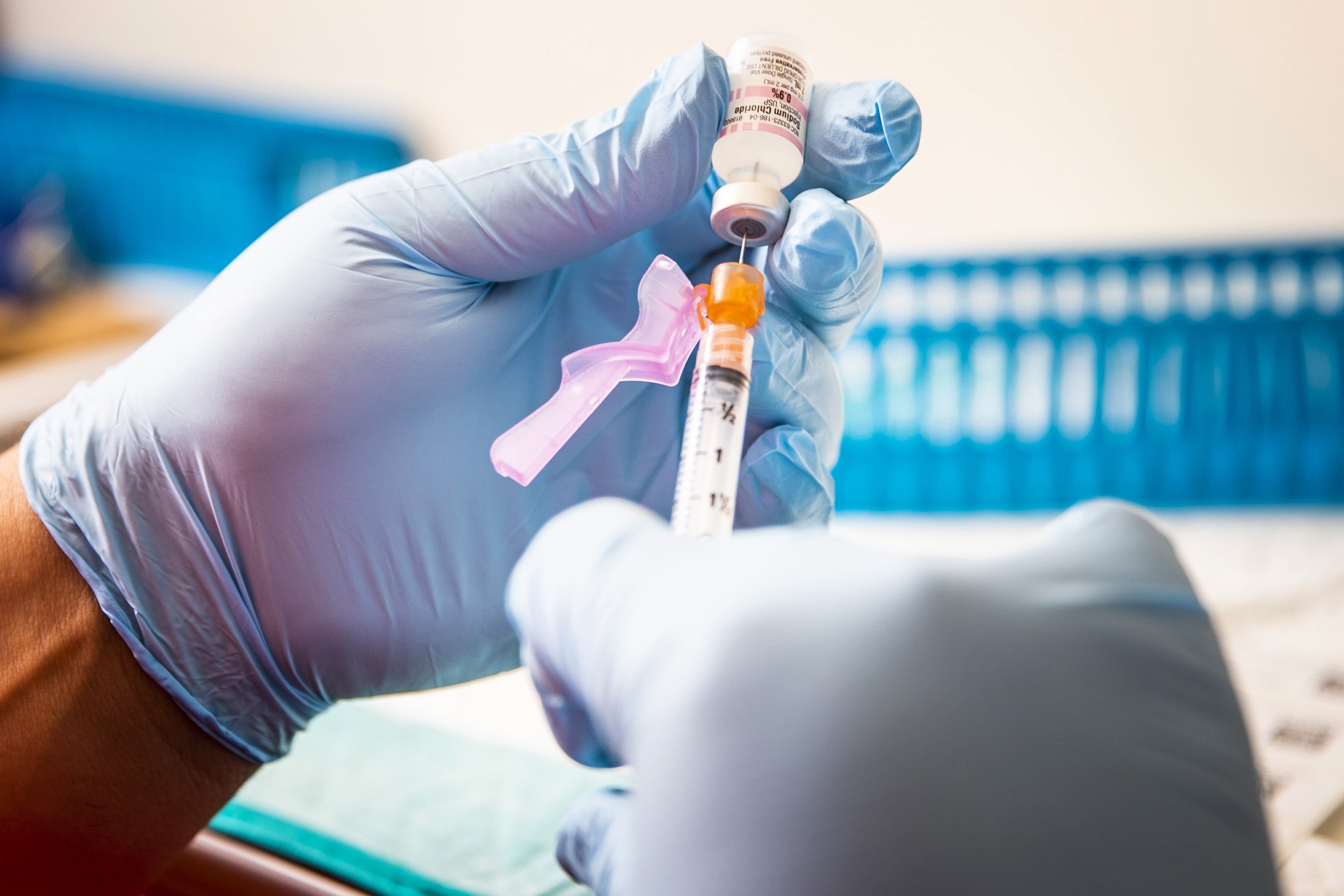
Quan chức FDA cho biết, sau khi cho phép sử dụng khẩn cấp, cơ quan này hy vọng sẽ nhanh chóng chuyển sang phê duyệt đầy đủ về vắc xin Covid cho trẻ em dưới 12 tuổi .
Sau khi cấp phép sử dụng khẩn cấp, cơ quan hy vọng sẽ nhanh chóng chuyển sang phê duyệt hoàn toàn
Ngày 16 tháng 7 năm 2021, 4:03 sáng +07 / Cập nhật ngày 16 tháng 7 năm 2021, 4:32 sáng +07
>> Vắc xin cho trẻ em dưới 12 tuổi
Bởi Erika Edwards
Ủy quyền khẩn cấp cho vắc xin Covid-19 ở trẻ em dưới 12 tuổi có thể đến từ sớm đến giữa mùa đông, Cục Quản lý Thực phẩm và Dược phẩm một quan chức cho biết hôm thứ Năm, một động thái có thể mang lại sự cứu trợ cho nhiều bậc cha mẹ đã không thể tiêm chủng cho con mình. Cơ quan này hy vọng sẽ nhanh chóng tiến tới việc phê duyệt hoàn toàn vắc xin cho nhóm tuổi này.
Quan chức này cho biết, một điểm mấu chốt đối với một số gia đình vẫn do dự là các loại vắc xin hiện đang được sử dụng được quản lý theo ủy quyền sử dụng khẩn cấp và chưa được FDA phê duyệt đầy đủ. Sự chấp thuận hoàn toàn, nếu nó đến nhanh chóng sau vòng khẩn cấp, có thể làm giảm bớt mối lo ngại đó.
Toàn bộ phạm vi bảo hiểm của đại dịch Covid-19
Vắc-xin Covid-19 chỉ được phép cho những người từ 12 tuổi trở lên ở Hoa Kỳ và chưa có vắc-xin nào nhận được sự chấp thuận đầy đủ.
Cả Moderna và Pfizer-BioNTech đều tung ra thử nghiệm vắc xin Covid-19 cho trẻ em dưới 12 tuổi vào tháng 3. Dự kiến sẽ có kết quả vào mùa thu, và các quan chức FDA sẽ mất thời gian để xem xét đơn đăng ký của các công ty dược phẩm.
Cơ quan quản lý đang yêu cầu 04 đến 06 tháng dữ liệu theo dõi an toàn cho trẻ em dưới 12 tuổi, quan chức FDA cho biết. Chỉ cần hai tháng dữ liệu theo dõi cho các thử nghiệm lâm sàng ở người lớn.
Dữ liệu bổ sung đó có thể giúp quá trình cấp phê duyệt đầy đủ dễ dàng hơn. Sáu tháng dữ liệu theo dõi là cần thiết cho những gì được gọi là đơn xin cấp phép sinh học, hoặc BLA.
Pfizer và Moderna đã nộp đơn xin cấp phép đầy đủ vắc-xin của họ cho người lớn từ 18 tuổi trở lên. Quan chức FDA cho biết việc cấp phép hoàn toàn cho người lớn là ưu tiên cao nhất của cơ quan này.
Pfizer cho biết trong một tuyên bố với NBC News rằng họ dự đoán kết quả thử nghiệm lâm sàng ở trẻ em từ 5 đến 11 tuổi vào tháng 9 và sau đó có thể xin phép sử dụng khẩn cấp. “Dữ liệu dành cho trẻ em 2 và dưới 5 tuổi có thể được cung cấp ngay sau đó”, công ty cho biết, đồng thời cho biết thêm rằng kết quả về trẻ em từ 6 tháng đến 2 tuổi có thể không được công bố cho đến tháng 10 hoặc tháng 11.
Tiến sĩ Buddy Creech, một trong những nhà nghiên cứu chính của thử nghiệm lâm sàng Moderna KidCOVE, bao gồm cả trẻ nhỏ từ 6 tháng tuổi, đã dự đoán một đợt triển khai dữ liệu nhi khoa tương tự như Pfizer.
“Tôi không thể tưởng tượng được, ngoại trừ có thể đối với những đứa trẻ từ 6 đến 11 tuổi, rằng chúng ta sẽ có quá nhiều dữ liệu trước cuối mùa thu”, Creech, cũng là một chuyên gia về bệnh truyền nhiễm ở trẻ em và là giám đốc của Vanderbilt Vaccine. Chương trình Nghiên cứu tại Trung tâm Y tế Đại học Vanderbilt ở Nashville, Tennessee, cho biết.
Ông nói thêm: Kết quả trên trẻ em từ 5 tuổi trở xuống có thể mất nhiều thời gian hơn. “Vẫn còn rất nhiều việc phải làm.”
Vắc xin an toàn và hiệu quả cho trẻ em là một công cụ quan trọng trong việc ngăn chặn sự lây lan của Covid-19, đặc biệt là với sự gia tăng nhanh chóng của biến thể delta dễ lây lan hơn.
Không có dấu hiệu nào cho thấy biến thể đang thay đổi của vi rút để có thể gây hại cho trẻ em nhiều hơn. Nhưng bản chất rất dễ lây lan của nó có nghĩa là những người chưa được tiêm phòng, bao gồm tất cả trẻ em dưới 12 tuổi, dễ bị tổn thương hơn.
Tiến sĩ Richard Besser, một bác sĩ nhi khoa và cựu quyền giám đốc của Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh cho biết: “Cho rằng trẻ em là một trong những nhóm không được tiêm chủng, chúng ta sẽ thấy nhiều trường hợp mắc bệnh hơn ở trẻ em. “Chúng ta sẽ thấy nhiều ca nhập viện hơn ở trẻ em, và không may là chúng ta sẽ thấy nhiều ca tử vong ở trẻ em hơn.”
Besser, hiện là chủ tịch của Quỹ Robert Wood Johnson, cho biết ông hy vọng FDA sẽ nhanh chóng tiến tới việc phê duyệt hoàn toàn vắc xin.
Ông nói: “Rất nhiều người nói rằng điều đó sẽ ảnh hưởng đến quyết định tiêm chủng của họ.
Một số bác sĩ về bệnh truyền nhiễm ở trẻ em không được thuyết phục hoàn toàn chấp thuận, chứ không phải là EUA, sẽ có nhiều tác động đến sự do dự của vắc xin.
Tiến sĩ Sean O’Leary, phó chủ tịch Ủy ban về các bệnh truyền nhiễm của Học viện Nhi khoa Hoa Kỳ cho biết: “Về cách vắc-xin được chấp thuận, không có nhiều sự khác biệt về chức năng” giữa việc cấp phép sử dụng khẩn cấp và phê duyệt hoàn toàn.
Tính đến ngày 8 tháng 7, hơn 4 triệu trẻ em đã được chẩn đoán mắc bệnh Covid-19, chiếm 14,2% tổng số trường hợp, theo Học viện Nhi khoa Hoa Kỳ. Theo dữ liệu mới nhất từ CDC, ít nhất 335 trẻ em từ 17 tuổi trở xuống đã chết vì Covid-19.
CHỈNH SỬA (16 tháng 7 năm 2021, 8:40 sáng ET): Phiên bản trước của bài báo này đã nêu sai số lượng nhà sản xuất thuốc đã nộp đơn xin phê duyệt đầy đủ từ FDA cho vắc xin Covid của họ. Đó là hai, Pfizer và Moderna, không chỉ Pfizer.
Theo NBCNEWS.COM
Xem Thêm: Các loại dầu nhớt GBOIL
Fanpage: GBOIL VIỆT NAM
GB OIL Việt Nam
Nhà nhập khẩu và phân phối tại Việt Nam | Công ty CP ĐT SX & Kinh doanh GB OIL.
Trụ Sở chính: 230 Cộng Hòa, Phường 12, Quận Tân Bình, Tp. Hồ Chí Minh Điện thoại: (028)39.300.878 – Fax: (028)39.305.795
CN Hà Nội: Tầng 2, Tòa Nhà PECO, Số 44, Phố Sài Đồng, Phường Sài Đồng, Quận Long Biên, Hà Nội. Điện thoại: (024)36.750.751 – Fax: (024)36.750.751
CN Đà Nẵng: Tầng 2-674A Điện Biên Phủ, TP. Đà Nẵng
Website: www.Gboil.vn – Email: sales@gboil.vn Hotline: 1900 2031